ייעוץ מקצועי:
ד"ר יקטרינה שולמן, מנהלת מרפאה אונקולוגית מרחבית, מחוז חיפה וגליל מערבי, מרכז רפואי כרמל;
ד"ר איהאב סמארה, רופא בכיר, מרפאה אונקולוגית מרחבית, מחוז חיפה וגליל מערבי, מרכז רפואי כרמל
מבוא
מטרתו של המידע המובא בהמשך הוא לשפוך על אבחון סרטן הוושט, סוגי הטיפולים, תופעות הלוואי וההתמודדות. עם זאת, מידע זה הוא כללי בלבד, ורק הצוות הרפואי המטפל בך ומכיר היטב את פרטי הרקע הרפואי שלך ואת נתוני מחלתך, יכול לייעץ לך בכל הנוגע לטיפול.
קראו בהרחבה: מהו סרטן.
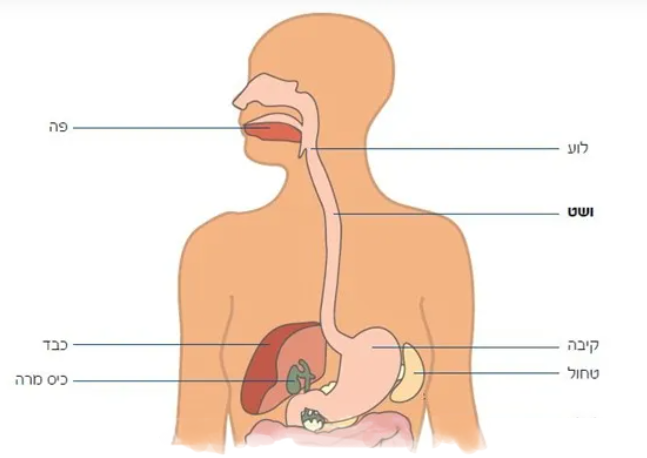
מבנה הוושט
הוושט (Esophagus) הוא צינור ארוך ושרירי המחבר בין הלוע לקיבה ומהווה חלק ממערכת העיכול. אורכו של הוושט בגופם של אנשים מבוגרים הוא כ-25 ס"מ. בזמן בליעת המזון שרירי הוושט מתכווצים כדי להעביר את המזון אל תוך הקיבה. החלק העליון של הוושט עובר מאחורי קנה הנשימה המחבר בין האף לריאות. האזור בו הוושט מתחבר לקיבה נקרא "מעבר ושט-קיבה".
ליד הוושט ישנן כמה בלוטות לימפה (שתפקידן להגן על הגוף מפני זיהומים, נגיפים ותאים סרטניים): בצוואר, באמצע החזה וליד נקודת המפגש עם הקיבה.
הוושט בנוי מארבע שכבות:
- רירית (מוקוזה) - השכבה הפנימית. שכבה לחה אשר מאפשרת למזון לנוע מטה לכיוון הקיבה.
- תת-רירית (סאב-מוקוזה) - שכבה זו כוללת בלוטות אשר מפרישות ריר ששומר על הלחות של הוושט.
- שרירי הוושט - שכבת השרירים שדוחפת את המזון לקיבה.
- השכבה החיצונית - שכבה זו מחברת בין הוושט לרקמות מסביבה.
סוגי סרטן הוושט
סרטן הוושט מהווה 1% מכלל סוגי הסרטן בישראל, וישנם שני סוגים עיקריים שמהווים כ-95% מהגידולים של סרטן זה:
- קרצינומה של תאי קשקש (Squamous cell carcinoma): גידול המתפתח בתאי הרירית אשר מרפדים את הוושט. גידול זה מתפתח בדרך כלל בחלקו העליון והאמצעי של הוושט.
- קרצינומה בלוטית, אדנוקרצינומה (Adenocarcinoma): גידול המתפתח בתאים של הבלוטות בתת-רירית. אדנוקרצינומה מתפתחת בדרך כלל בחלקו התחתון של הוושט, כולל במעבר ושט-קיבה.
קביעת סוג המחלה מסייעת לרופא לתכנן את הטיפול הטוב ביותר.
קיימים גידולים אחרים, נדירים יותר, כגון גידולים נוירואנדוקריניים בעלי רמת התמיינות נמוכה, לימפומה, סרטן מסוג תאים קטנים וסרקומה של רקמות רכות, כגון GIST. הטיפול בסוגים הנדירים של סרטן הוושט שונה מהטיפולים המתוארים בדף מידע זה. למידע נוסף ניתן לפנות בשיחת חינם ל"טלמידע" של האגודה למלחמה בסרטן, בטל': 1-800-599-995
גורמי סיכון
סרטן הוושט הוא מחלה נדירה יחסית, אך שכיחותה עולה עם הזמן. הגורמים לסרטן הוושט אינם ידועים, אך ישנם גורמים שיכולים להעלות את הסיכון למחלה:
גורמי סיכון הניתנים לשינוי (קשורים לאורח חיים)
- עישון: הסיכון לסרטן ושט עולה ככל שמעשנים זמן רב יותר, ובתדירות רבה יותר. עישון מכל סוג הוא מזיק: סיגריות, מקטרת, סיגרים, נרגילה וסיגריה אלקטרונית.
- השמנת יתר: עודף משקל ובעיקר השמנה בטנית, יכולים להעלות את הסיכון להתפתחות סרטן הוושט, בייחוד אדנוקרצינומה. זאת משום שהשמנה בטנית יכלה להוביל לעליית לחץ תוך-בטני שגורם לריפלוקס, המהווה זרז לאדנוקרצינומה של הוושט.
- אלכוהול: שתייה מרובה של אלכוהול למשך זמן רב מעלה את הסיכון לסרטן הוושט. שתיית אלכוהול ועישון במקביל מגבירים עוד יותר את הסיכון לחלות.
- תזונה: צריכה מוגברת של בשר אדום ובשר מעובד (כגון נקניקיות והמבורגרים) יכולה להעלות את הסיכון. כדי להפחית את הסיכון מומלץ לצרוך כמויות גדולות של ירקות ופירות.
- שתייה חמה: ישנן עדויות לפיהן שתייה של משקאות חמים (בטמפרטורה של כ-65 מעלות צלזיוס ומעלה) יכולה לעלות את הסיכון לחלות, זאת מכיוון שנוזל חם מאוד יכול לפגוע בדופן הוושט.
- חוסר פעילות גופנית: גורם סיכון אפשרי הקשור לסוגי סרטן שונים במערכת העיכול, כולל סרטן הוושט, אם כי נכון להיום, אין מספיק הוכחות לקשר ישיר.
גורמי סיכון נוספים
- החזר תוכן חומצי במשך זמן רב: מצב אופייני לאנשים הסובלים מ"ריפלוקס קיבתי-ושטי" (חזרת תוכן הקיבה או חלק ממנו אל הוושט – Gastro Esophageal Reflux Disease-GERD). ריפלוקס חומצי עלול לפגוע בוושט ולגרום למצב רפואי הנקרא "ושט על שם בארט" (Barrett's Esophagus). במצב זה תאים לא תקינים מתפתחים בציפוי בקצהו התחתון של הוושט. זהו אינו גידול סרטני, אולם עם הזמן הוא עלול להתפתח במקרים נדירים (פחות מ-1 ל-100) לסרטן ושט מסוג בלוטי (אדנוקרצינומה).
- מגדר: סרטן הוושט נפוץ פי שניים בקרב גברים מאשר בנשים.
- גיל: הסיכון לסרטן הוושט עולה עם הגיל. המחלה אינה נפוצה מתחת לגיל 45.
- טיפולים נגד מחלת סרטן קודמת: במקרים נדירים מאוד קרינה (רדיותרפיה) לאזור החזה יכולה להעלות את הסיכון לסרטן הוושט.
- אכלזיה (Achalasia): מצב שבו השרירים השולטים על הפתח בין הוושט לקיבה אינם פועלים כראוי ואינם מאפשרים התקדמות המזון, כך שמזון מצטבר בוושט ואינו מגיע לקיבה.
- תסמונת פלאמר-וינסון (Plummer-Vinson syndrome): תסמונת נדירה אשר עלולה לגרום לבעיות במעבר המזון לקיבה וגירוי כרוני באזור המזון הכלוא. כ-1 מכל 10 אנשים עם תסמונת זו מפתחים בסופו של דבר סרטן תאי קשקש של הוושט או סרטן בחלק התחתון של הגרון (היפופרינקס).
- טילוזיס (Tylosis): מחלה תורשתית נדירה כתוצאה משינויים בגן RHBDF2. הסובלים ממחלה זאת מפתחים, בין היתר, גם גידולים קטנים שפירים (פפילומות) בוושט, והם נמצאים בסיכון גבוה יותר לסרטן ושט.
- תסמונת בלום (Bloom Syndrome): נגרמת עקב שינויים בגןBLM אשר יש לו תפקיד חשוב ביצירת חלבון שאחראי על יציבות חלוקת תאים. נשאי תסמונת בלום נמצאים בסיכון גבוה יותר לחלות בסרטן ושט מסוג תאי קשקש.
- נגיף הפפילומה (HPV): נגיף הפפילומה הוא גורם סיכון לסוגי סרטן שונים באזור הראש והצוואר, והוא נחשב גורם סיכון אפשרי לסרטן ושט סוג תאי קשקש (יפורט בהמשך), אם כי היום אין מספיק הוכחות לקשר ודאי.
האם ניתן למנוע סרטן ושט?
לא ניתן למנוע את כל סוגי סרטן הוושט, אך ניתן להפחית את הסיכון על ידי הימנעות מעישון ואלכוהול, שמירה על משקל תקין, תזונה עשירה בפירות וירקות, וטיפול ומעקב במצבי ריפלוקס.
גילוי מוקדם של סרטן הוושט
נכון להיום אין תוכנית סקר כללית לאיתור מוקדם של סרטן הוושט לכלל האוכלוסייה עם זאת, מומלץ לבצע בדיקות מעקב לאנשים הנמצאים בסיכון גבוה, למשל הסובלים מ־Gastroesophageal Reflux Disease ממושך או מאובחנים עם Barrett's Esophagus שכן גילוי מוקדם של מצבים טרום-סרטניים יכול למנוע התפתחות סרטן חודרני.
בדיקת המעקב העיקרית היא גסטרוסקופיה (אנדוסקופיה של הוושט והקיבה), המאפשרת לזהות שינויים טרום-סרטניים ולעיתים גם לקחת ביופסיה.
תסמינים (סימפטומים) של סרטן ושט
סרטן הוושט עלול לגרום לתסמינים הבאים:
- קושי בבליעה (דיספאגיה) הוא התסמין הנפוץ ביותר של סרטן הוושט. לרוב תיתכן תחושה שהמזון נתקע בדרכו לקיבה, גם אם בתחילה נוזלים שונים נבלעים היטב. ייתכנו גם כאבים בזמן הבליעה.
- ירידה במשקל או כאב ואי-נוחות מאחורי עצם החזה או בגב.
- הקאות או מצב שבו המזון עולה חזרה לפני ההגעה לקיבה.
- צרבות שאינן חולפות.
- שיעול ו/או צרידות בקול הנובעים מלחץ על עצב הקול.
- כאב מאחורי עצם החזה או בגרון, לחץ או צריבה בבית החזה.
חשוב לזכור: הופעת התסמינים הללו אינה מעידה בהכרח על סרטן, אך היא מחייבת פנייה מיידית לבדיקה רפואית. אל תחכו שהתסמינים יחלפו מעצמם. גילוי מוקדם מציל חיים.
אבחון סרטן ושט
בירור האבחנה מתחיל על פי רוב בביקור אצל רופא/ת המשפחה, שיבדוק ויחליט אם יש להפנותך לרופא מומחה. הרופאים בבית החולים או במרפאת המומחים יתעדו את ההיסטוריה הרפואית ויבצעו בדיקה גופנית. ייתכן שיערכו בדיקות דם וצילום רנטגן של החזה כדי לבדוק את מצב הבריאות הכללית. ישנן בדיקות רבות המשמשות לאבחון סרטן הוושט. לא כל הבדיקות המתוארות כאן ישמשו עבור כל אדם. הצוות הרפואי עשוי לשקול את הגורמים הבאים בעת בחירת בדיקת אבחון:
- סוג הסרטן המשוער.
- הסימנים והתסמינים.
- הגיל ומצב הבריאות הכללי.
- תוצאות בדיקות רפואיות קודמות.
בנוסף לבדיקה גופנית, קיימות כמה בדיקות מקובלות לצורך אבחון המחלה:
בדיקות הדמיה
אנדוסקופיה/אסופאגוסקופיה (Esophagoscopy)
בדיקה אנדוסקופית היא בדיקה פולשנית המאפשרת הסתכלות אל פנים הגוף. שם הבדיקה משתנה לפי האזור או האיבר הנבדק בגוף. הסתכלות אל תוך הוושט נקראת "אסופאגוסקופיה". בדיקה זו מאפשרת לרופא להסתכל ישירות אל תוך הוושט באמצעות צינורית דקה וגמישה הנקראת אנדוסקופ. בקצהו של האנדוסקופ ממוקמת מצלמה זעירה, המלווה במקור אור. במידת הצורך יכול הצוות הרפואי לקחת דגימה קטנה של תאים (ביופסיה) לצורך בדיקה מיקרוסקופית, באמצעות צבת קטנה הנמצאת גם היא בקצה האנדוסקופ. בדיקת הביופסיה תוכל לאשר אם מדובר בגידול ממאיר או שפיר. אסופאגוסקופיה מתבצעת בדרך כלל במרפאות חוץ ומחייבת צום של ארבע שעות לפחות לפני ביצוע הבדיקה. כדי למנוע אי נוחות מהחדרת צינורית האנדוסקופ, ייתכן שלפני הבדיקה תינתן הרדמה מקומית באמצעות התזת תרסיס אל עומק הגרון או טשטוש בחומר הרדמה המוזרק לווריד. לעיתים נדרשת הרדמה כללית לשם ביצוע הבדיקה, ובמקרה זה הבדיקה לרוב כרוכה באשפוז ללילה אחד בבית החולים.
הבדיקה אינה נעימה, אך אינה אמורה לגרום לכאב. במקרה של הרדמה מקומית או טשטוש, ניתן לחזור הביתה כעבור כמה שעות, לאחר שהשפעת חומר ההרגעה תפוג. מומלץ שלא לנהוג במשך כמה שעות לאחר הבדיקה, ועל כן כדאי לבוא לבדיקה עם מלווה. אין לבלוע דבר במשך כשעה לאחר הבדיקה, עד שהשפעת ההרדמה המקומית תפוג. לעיתים יש תחושה של כאב בגרון לאחר ההליך. זוהי תחושה נורמלית לחלוטין, והיא אמורה לחלוף בתוך יום-יומיים. אם הכאב אינו חולף, יש ליצור קשר עם הצוות המטפל בבית החולים. כמו כן, חשוב לדווח לצוות אם מופיעים כאבים בחזה במהלך או לאחר הבדיקה.
אולטרה-סאונד אנדוסקופי (Endoscopic Ultra-Sound-EUS)
בדיקה זו זהה לבדיקת האסופאגוסקופיה למעט פרט אחד: בקצה צינורית האנדוסקופ מותקן חיישן אולטרה-סאונד זעיר. בדיקת אולטרה-סאונד עושה שימוש בגלי קול כדי לבחון את האזור המדובר. הבדיקה מאפשרת לרופא לבדוק היטב את שכבת דופן הוושט והאזורים הסמוכים לה, ולקבוע את עומק חדירת הגידול אל הדופן. בעזרת הליך זה ניתן לקבל תמונת מצב מדויקת יותר של הגידול. הבדיקה מאפשרת גם להבחין אם בלוטות הלימפה באזור מוגדלות. גם בבדיקה זו מתאפשרת נטילת ביופסיה.
צילום בריום
באמצעות שימוש במכשיר הרנטגן הרופא יכול לצפות בתמיסת בריום הניתנת לבליעה כאשר היא יורדת לאורך הוושט לכיוון הקיבה. באותו הזמן מצולמות תמונות רנטגן של הוושט. הליך זה נמשך כ-15 דקות ואינו כרוך בכאב. בדרך כלל משתמשים בבדיקה זו כחלק מתכנון הטיפול הקרינתי. הבדיקה אינה בשימוש שגרתי.
סריקת CT (טומוגרפיה ממוחשבת, Computerized Tomography)
בדיקת הדמיה היוצרת תמונה תלת-ממדית של פנים הגוף. הבדיקה במקרה זה מיועדת למי שאינו עושה בדיקת PET-CT. הבדיקה אינה כרוכה בכאב, והיא נמשכת בין 10 ל-30 דקות. לפני הבדיקה יש להימנע מאכילה ומשתייה במשך ארבע שעות לפחות. ייתכן שתתבקש לשתות חומר ניגוד (יוד) או שתקבל זריקה של החומר, הצובע אזורים מסוימים בגוף ומדגיש אותם בסריקה. ברוב המקרים ניתן לחזור הביתה מיד עם תום הבדיקה.
בדיקת PET-CT
בדיקה המשלבת סריקת CT יחד עם סריקת PET ((Positron Emission Tomography ומעניקה מידע מפורט יותר על האזור הנבדק. בנוסף, הבדיקה עשויה לספק מידע אשר יסייע לרופאים בתכנון הטיפול המתאים ביותר. לפני הבדיקה יש להימנע מאכילה במשך שש שעות (שתייה מותרת). חומר רדיואקטיבי (FDG) בכמות קטנה מוזרק לתוך הווריד, בדרך כלל בזרוע. הסריקה מתבצעת לאחר המתנה של שעה אחת לפחות, ונמשכת בין 30 ל-90 דקות.
לפרוסקופיה
בדיקה הכרוכה בניתוח קטן שמתבצע בהרדמה כללית. הבדיקה מאפשרת לרופא להתבונן בחלל הבטן, במטרה לבדוק אם הגידול הסרטני התפשט לאיברים נוספים. הרופא יבצע חתך קטן (כשני ס"מ) בעור ובשריר ליד הטבור, ויחדיר צינורית פיברו-אופטית גמישה ודקה (לפרוסקופ) לתוך הבטן. הרופא יוכל לבחון את האזור ולקחת דגימות רקמה (ביופסיות) שאותן ניתן לבחון תחת מיקרוסקופ. הצורך בביצוע בדיקה זו תלוי במיקום הגידול הסרטני בוושט. לרוב ניתן להשתחרר מבית החולים כאשר השפעת ההרדמה פגה, אך לעיתים יש צורך להישאר לאשפוז במשך הלילה.
דגימת רקמה (ביופסיה)
לצורך אבחון מחלת סרטן, לרוב יש לבצע ביופסיה - הליך פולשני שבו רופא נוטל דגימה מהרקמה החשודה. רופא פתולוג מסתכל על הרקמה תחת מיקרוסקופ ומבצע בדיקות נוספות, כדי לבחון אם הרקמה ממאירה. דו"ח הפתולוגיה ממלא תפקיד חשוב באבחון סרטן ובקביעת אפשרויות הטיפול. ברוב המקרים פענוח הבדיקה מגיע לרופא כעבור כמה שבועות. עם קבלת התוצאות חשוב לדון עליהן עם הרופא. לעיתים מתבצעת ביופסיית מחט המונחית ב-CT. בעזרת בדיקת ה-CT ניתן לאתר במדויק את הרקמה החשודה שממנה יש ליטול דגימה.
בדיקת סמנים ביולוגיים של הגידול
הרופא עשוי להמליץ על ביצוע בדיקה מולקולרית של הגידול - בדיקות מעבדה נוספות לדגימת גידול (ביופסיה) כדי לזהות גנים ספציפיים, חלבונים וגורמים אחרים ייחודיים לגידול. התוצאות של בדיקות אלה יכולות לעזור לקבוע את אפשרויות הטיפול.
בדיקת MSI-H/dMMR – בתאים רגילים מתקיים תהליך שנקרא "תיקון אי התאמה" (MMR) והוא מתקן שגיאות (כגון מוטציות) שיכולות לקרות כאשר הדנ"א מתחלק ויוצר עותק של עצמו. אם מערכת ה-MMR של התא לא פועלת כמו שצריך, שגיאות יצטברו ויגרמו לדנ"א להפוך ללא יציב. מצב זה נקרא "אי-יציבות מיקרו-לוויין" (MSI).
ישנם שני סוגי בדיקות עבור סמן ביולוגי זה. בהתאם לסוג הבדיקה שבה נעשה שימוש, תוצאה חריגה נקראת "אי-יציבות מיקרו-לוויין גבוהה "(MSI-H) או חסר התאמה לתיקון (dMMR). שתי התוצאות אומרות אותו דבר.
בדיקת HER2 - הבדיקה מיועדת לזיהוי ביטוי יתר של קולטן לצמיחה של האפידרמיס האנושי 2 (HER2), שהוא חלבון מיוחד שנמצא על פני השטח של תאים. הבדיקה רלוונטית לגידולים במעבר ושט-קיבה ולא לגידולים בכל מיקום לאורך הוושט.
כאשר בגידול יש רמות גבוהות של HER2, הן יכולות להניע את הצמיחה שלו ולהתפשט. סוגים אלה של סרטן מכונים HER2 חיובי, וקיימים טיפולים מכוונים כנגדם (פרטים בפרק טיפול ביולוגי).
בדיקת CPS (מדד PD-L1 ) - מיועדת לזיהוי רמת הביטוי של PD-L1 על גבי תאי הגידול שנלקחו בביופסיה כדי לבחון התאמה לטיפולים אימונותרפיים (פרטים בפרק אימונותרפיה).
בדיקת Claudin 18.2 (CLDN18.2) - בדיקה המיועדת לזהות נוכחות של חלבון בשם Claudin 18.2 על פני תאי הגידול. חלבון זה מהווה רכיב במבנה התא, ובמקרים של סרטן הוושט ומעבר הוושט-קיבה (GEJ) מסוג אדנוקרצינומה, זיהוי רמה גבוהה של חלבון מאפשר התאמת טיפול ביולוגי ממוקד מטרה (פרטים בפרק טיפול ביולוגי).
במקרים מסוימים, בדיקות מולקולריות רחבות עשויות לזהות שינויים גנטיים ספציפיים ונדירים בגידול, המאפשרים התאמת טיפול ביולוגי מדויק (פרטים בפרק טיפול ביולוגי).
בדיקה לאבחון חסר פעילות האנזים DPD
לפני תחילת הטיפול בפלואורואורציל (תרופה כימית המוזכרת בהמשך בפרק הטיפול הכימי) יש לבצע בדיקת דם לחוסר פעילות, היעדר חלקי או מלא של האנזים Dihydropyrimidine Dehydrogenase) DPD) בגוף. אנזים זה עוזר לגוף לפרק פלואורואורציל. באנשים עם רמות DPD נמוכות או ללא DPD כלל קיים סיכון מוגבר לתופעות לוואי חמורות או מסכנות חיים מהתרופה פלואורואורציל. חוסר מוחלט באנזים DPD הוא נדיר מאוד, אך לפי ההערכות כ-8-3% מהאוכלוסייה סובלים מחוסר חלקי באנזים. חוסר זה אינו מתבטא בסימפטומים כלשהם וניתן לגילוי רק בבדיקת דם. . אם מתגלה חוסר באנזים DPD הרופא המטפל עשוי להמליץ על טיפול במינון נמוך יותר של פלואורואורציל או על החלפת הטיפול בתרופה כימותרפית שונה.
המתנה לתוצאות הבדיקות
ייתכן שיחלפו כמה ימים או כמה שבועות עד שכל תוצאות הבדיקות יתקבלו ועד פגישת העדכון עם הרופא או הרופאה. תקופת ההמתנה עלולה להיות מלווה בחששות ובמתח, לכן מומלץ להיעזר במשפחה או בסביבה הקרובה בשביל תמיכה וסיוע.
אינך לבד! ניתן להיעזר במוקד 'טלתמיכה'® של האגודה למלחמה בסרטן - מוקד טלפוני בעברית וברוסית, המעניק סיוע מיידי ראשוני לחולי וחולות סרטן ולקרוביהם הנמצאים במצוקה נפשית וזקוקים לתמיכה ולאוזן קשבת. צוות המוקד מפנה לטיפול בבית החולים או בקהילה לפי הצורך. טל': 1-800-200-444.
קביעת שלב ודרגת המחלה
שלב המחלה
"שלב המחלה" הוא מונח המתאר את מידת התפשטות המחלה. לקביעת שלב המחלה יש תפקיד חשוב בהחלטה על הטיפול המתאים והיעיל ביותר. שיטה הנותנת מידע מדויק על שלב המחלה היא שיטת TNM:
T (Tumor) - מתאר את היקף וגודל הגידול הסרטני הראשוני.
T1 - הגידול התפשט לשכבה הפנימית (רירית או תת-רירית) של הוושט.
T2 - הגידול התפשט לשכבת השרירים של הוושט.
T3 - הגידול התפשט לשכבה החיצונית של הוושט.
T4 - הגידול התפשט לרקמות סמוכות, שלב זה מתחלק לשני שלבים נוספים:
T4a - הגידול התפשט לקרום הריאות, קרום הלב או הסרעפת.
T4b - הגידול התפשט לאיברים סמוכים, כגון צינור הנשימה (הטרכיאה), עמוד השדרה או עורקי דם מרכזיים.
N (Nodes) - מתאר את מידת התפשטות הגידול לבלוטות הלימפה הסמוכות.
N0 - אין תאים סרטניים באף אחת מבלוטות הלימפה.
N1 - ישנם תאים סרטניים ב-2-1 בלוטות לימפה.
N2 - ישנם תאים סרטניים ב-6-3 בלוטות לימפה.
N3 - ישנם תאים סרטניים ב-7 או יותר בלוטות לימפה.
אם תאים סרטניים התפשטו לבלוטות הלימפה, מציינים כי "הבלוטות חיוביות".
M (Metastasis) - מתאר את מידת התפשטות הגידול הסרטני לחלקים אחרים בגוף, כגון הכבד או הריאות.
M0 - מתאר מצב שבו לא נמצאו גרורות.
M1 - מתאר מחלה גרורתית שהתפשטה לאיברים נוספים.
דרגת הגידול
דרגת הגידול תלויה במראה התאים תחת מיקרוסקופ. באופן כללי, ציון נמוך מצביע על סרטן שגדל לאט יותר וציון גבוה יותר מצביע על סרטן שגדל מהר יותר. שיטת הדירוג שבה משתמשים בדרך כלל היא:
דרגה 1 - תאים סרטניים הדומים לתאים רגילים ואינם גדלים במהירות.
דרגה 2 – תאים סרטניים שאינם נראים כמו תאים רגילים וגדלים מהר יותר מתאים רגילים.
דרגה 3 - תאים סרטניים שנראים לא תקינים ועשויים לגדול או להתפשט בצורה אגרסיבית יותר.
תיאור שלבי המחלה
הצוות הרפואי מסכם את שלב המחלה ע"י שילוב של שיטת TNM עם קביעת דרגת הגידול.
שלב 0 - קרוי בשם קרצינומה מקומית (אין-סיטו - CIS, Carcinoma In Situ) או דיספלזיה בדרגה גבוהה (High Grade Dysplasia) - זהו שלב מוקדם מאוד של סרטן הוושט. בשלב זה ישנם תאים סרטניים במעטפת הוושט, אולם הם מתרכזים רק בתוכה. סרטן הוושט אינו מאובחן בדרך כלל בשלב כה מוקדם, כיוון שאין כלל תסמינים בשלב זה. אם תאים אלו לא יטופלו, הם עלולים להתפתח לסרטן חודרני.
שלב IA - הסרטן נמצא רק בשכבה הפנימית של הוושט, ולא התפשט לרקמות סמוכות, בלוטות לימפה סמוכות או איברים סמוכים.
שלב IB - בשלב זה הגידול הסרטני התפשט לתוך השכבה השרירית של קיר הוושט או התפשט לבלוטות לימפה סמוכות, אך לא התפשט לאף איבר נוסף.
שלב IIA - הסרטן התפשט מחוץ לשכבה החיצונית של הוושט, אך לא התפשט לבלוטות לימפה סמוכות או לאיברים אחרים
שלב IIB - הגידול נמצא בשתי השכבות העליונות של הוושט והתפשט ל-2-1 בלוטות לימפה. הגידול לא התפשט לאיברים אחרים.
שלב IIIA - אחת משלוש האפשרויות הבאות:
- הגידול התפשט לקרום הריאות, קרום הלב, או לשכבת השריר מתחת לריאות, אך לא התפשט לבלוטות לימפה או רקמות אחרות. או
- הגידול התפשט לשכבה החיצונית של הוושט ול- 2-1 בלוטות לימפה, אך לא לאיברים אחרים. או
- הגידול התפשט לשתי השכבות החיצוניות של הוושט, ול-6-3 בלוטות לימפה, אך הגידול לא התפשט לאיברים אחרים.
שלב IIIB - הגידול התפשט לשכבה החיצונית של הוושט ול-6-3 בלוטות לימפה, אך לא התפשט לאף איבר אחר
שלב IIIC - אחת משלוש האפשרויות הבאות:
- הגידול התפשט לקרום הריאות, קרום הלב, או לשכבת השריר מתחת לריאות, ולבלוטות הלימפה - לא יותר משש בלוטות.
- או הגידול התפשט לרקמות סמוכות, כגון קנה הנשימה או עמוד השדרה, ולבלוטות לימפה כלשהן.
- או גידול בכל גודל שהוא, שהתפשט לשבע בלוטות לימפה או יותר, אך לא לאיברים אחרים.
שלב IV - הגידול התפשט לבלוטות הלימפה ולאיברים אחרים בגוף, כגון: הכבד, הריאות, חלל הבטן.
תכנון הטיפול
תכנון הטיפול המיטבי ייעשה, בדרך כלל, על ידי צוות רב־תחומי הכולל רופאים ורופאות מתחומי הכירורגיה, הרדיולוגיה, הפתולוגיה והאונקולוגיה. ההחלטה על טיפול בסרטן הוושט היא מורכבת ודורשת שיתוף פעולה בין חברי הצוות. ישנם צוותים נוספים בבית החולים שיכולים לסייע לפי הצורך בתחומים כגון תזונה, פיזיותרפיה ומתן שירותים סוציאליים שונים, המסייעים בהתמודדות עם המחלה והטיפול . כדי לתכנן את הטיפול הטוב ביותר עבורך, הם יתחשבו בכמה גורמים, לרבות הגיל והמצב הבריאותי הכללי של החולה, סוג המחלה, בשלב ובדרגה שלה (כלומר, במיקום הגידול, היקפו ומידת התפשטותו ברחבי הגוף).
במסגרת תכנון הטיפול, הרופא או הרופאה המטפלים ישוחחו עם החולה על דרך הטיפול המתאימה ביותר, או יציעו לבחור בטיפול אחד מבין כמה אפשרויות. אם יש צורך להחליט על דרך טיפול אחת, חשוב לוודא שתקבלו כל המידע על דרכי הטיפול האפשריות. ניתן לשאול את הצוות הרפואי כל שאלה בנוגע לטיפול ולתופעות הלוואי. לעיתים קרובות הכנת שאלות מראש ונוכחות של אדם קרוב (חבר/ה או בן או בת משפחה) בפגישה עם הצוות הרפואי עוזרות לברר את כל הפרטים ולזכור את תוכן הפגישה.
יתרונות הטיפול וחסרונותיו
אנשים רבים חוששים מהטיפולים נגד מחלת הסרטן בשל תופעות הלוואי האפשריות, אבל לרוב ניתן לשלוט בתופעות הלוואי באמצעות תרופות. חשוב לזכור שהטיפול מותאם באופן אישי לכל אדם שחלה, והוא משתנה בהתאם למחלתו הראשונית ולמצבו הכללי.
כאשר מטרת הטיפול היא לרפא את המחלה או לשלוט בגידול לאורך זמן, ההחלטה אם לקבל אותו תהיה קלה יותר, ככל הנראה. עם זאת, יש לשקול את יתרונות הטיפול לעומת חסרונותיו. אם אין אפשרות ריפוי, והטיפול נועד להאט את התקדמות המחלה או לעצור אותה לתקופת זמן מסוימת, יהיה קשה יותר להחליט אם להסכים לקבל אותו.
בנסיבות כאלו קבלת ההחלטות הנוגעות לטיפול היא תמיד קשה, וכדאי לדון על כך בפירוט עם הרופא המטפל. גם אם בוחרים שלא לקבל טיפול, אפשר לקבל טיפול לשליטה בתסמינים. טיפול זה נקרא טיפול תומך או טיפול פליאטיבי.
חוות דעת רפואית נוספת
צוות רב־תחומי של מומחים יקבע מהו הטיפול המתאים ביותר, אבל בהחלט אפשר לבקש חוות דעת רפואית נוספת, וזו הזכות המלאה של כל אדם על פי סעיף 3 לחוק זכויות החולה, תשנ"ו־1996: "מטופל זכאי להשיג מיוזמתו דעה נוספת לעניין הטיפול בו; המטפל והמוסד הרפואי יסייעו למטופל בכל הדרוש למימוש זכות זו".
בעת קבלת חוות דעת נוספת, כדאי להכין מראש רשימת שאלות ולהגיע בלוויית חבר/ה או בן/בת משפחה על מנת לזכור ולתעד את פרטי הפגישה.
מתן הסכמה מדעת
לפני קבלת טיפול כלשהו הצוות הרפואי יסביר לך על סוג הטיפול והיקפו, על מטרותיו, על יתרונותיו וחסרונותיו, על סיכונים ותופעות לוואי ועל טיפולים אפשריים אחרים. לאחר מכן יש לחתום על טופס הסכמה מדעת – מסמך הצהרה שבו מובעת הסכמה לקבל את הטיפול מהצוות הרפואי. לא יינתן לך טיפול רפואי ללא הסכמתך וללא חתימתך על הטופס.
תזונה לפני תחילת טיפול
לאחר האבחון חשוב להיפגש עם תזונאי/ת כדי לקבל הסבר על ההכנה לטיפולים הצפויים. במקרים רבים כאשר יש גידול בוושט קיימים קשיי אכילה, ותיתכן גם ירידה במשקל. ליווי של תזונאי לאורך המחלה חשוב כדי למנוע ככל הניתן איבוד משקל.
חשוב להקפיד על תזונה מאוזנת עד כמה שניתן לפני תחילת הטיפולים, ויש ליטול תוספי תזונה במידת הצורך. אכילה מוגברת בשלב זה תעזור להאט את הירידה במשקל, ויכולה גם לעזור בהתמודדות עם הטיפולים בהמשך.
במקרה של קושי בבליעה, מומלץ לאכול מספר ארוחות קטנות במשך היום ולצרוך מזון רך. אם אין אפשרות לבלוע כלל, חשוב לגשת מיד למרכז הרפואי.
טיפולים אנדוסקופיים
טיפול באמצעות שיטות אנדוסקופיות יכול לשמש טיפול סופי (לצורך פתרון) במקרים של מצבים טרום-סרטניים או סרטן בשלב התחלתי, או לצורך הרחבת הוושט במקרים שבהם הגידול חוסם את הוושט ומפריע לבליעה. בטכניקה זו חלק מהרירית הפנימית של הוושט מוסרת בעזרת מכשירים המחוברים לאנדוסקופ. לעיתים נעשה שימוש בתומכן פנימי לצורך הרחבה.
לאחר הטיפול האנדוסקופי המטופל יקבל המלצות והנחיות מהרופא אם יש צורך בטיפול תרופתי משלים.
טיפול פוטודינמי
טיפול פוטודינמי עושה שימוש בקרן לייזר המשולבת עם תרופה רגישה לאור כדי להרוס תאים לא תקינים. התרופה הופכת לפעילה רק בהשפעת האור, ולכן רק תאים סרטניים הנמצאים על פני שטח הגידול יגיבו. עם זאת, התרופה יכולה להצטבר בתאים הבריאים, לכן חשוב להימנע מחשיפה לאור במשך 4 עד 6 שבועות.
טיפול זה מבוצע רק בחלק מהמרכזים הרפואיים, והוא ניתן בעיקר במצבים טרום-סרטניים כגון תסמונת "ושט על שם בארט" או בגידולי ושט בשלבים התחלתיים, או בגידולים גדולים שחוסמים את המעבר, כדי להרוס תאים על פני שטח הגידול ולהקל את הבליעה. לאחר הטיפול תיתכן נפיחות בוושט אשר תקשה את הבליעה, אך היא צפויה לחלוף בתוך כמה ימים. הטיפול עצמו עלול לגרום להיצרות של הוושט ולעיתים יש צורך בפעולות הרחבה.
צריבה באמצעות גז ארגון ( Argon Plasma Coagulation - APC)
שיטה הגורמת לקרישה של פלסמה בתאי הגידול וע"י כך לגרימת מוות תאי. השיטה בשימוש במקרים שבהם הגידול אינו נתיח ויש הפרעה בבליעה עקב חסימה.
אבלציה באמצעות גלי רדיו (Radiofrequency Ablation - RFA)
שיטה המאפשרת להשמיד תאים סרטניים בחום הנוצר על ידי גלי רדיו.
ניתוח אנדוסקופי לכריתה תת-רירית (Endoscopic Mucosal Resection - EMR)
בסרטן ושט בשלב מוקדם מאוד שמאובחן בתוך השכבה הפנימית של הוושט (הרירית), ניתן לטפל לפעמים באמצעות אנדוסקופ. הרופא מחדיר אנדוסקופ ובוחן את האזור הנגוע. במהלך הפעולה הרופא יכול להוציא את התאים הנגועים מהשכבה הרירית של הוושט.
תופעות הלוואי הנפוצות ביותר לאחר EMR הן דימום והצרה של הוושט. קיים סיכון קטן ביותר לקריעה של קיר הוושט.
הרחבת הוושט ע"י בלון
הרופא משתמש בבלון אנדוסקופי כדי להרחיב את הוושט ולהגדיל את המרווח שבו עוברים המזון והנוזלים. הליך זה נעשה לעיתים קרובות לאחר טיפול בקרינה או לאחר ניתוח, ולעיתים יש צורך לחזור עליו יותר מפעם אחת. ההרחבה היא פשוטה ומהירה. מבצע אותה גסטרואנטרולוג בזמן גסטרוסקופיה, בהרדמה מקומית או כללית.
הכנסת תומכן (Stent)
בטיפול זה מוחדר צינור רשת מפלסטיק, מתכת או תיל הנקרא "תומכן" לתוך הוושט בעזרת אנדוסקופ, בתהליך הדומה לאסופאגוסקופיה. הצינור מסייע למנוע את היצרות הוושט ומאפשר מעבר של מזון בקלות רבה יותר. עם זאת, חשוב לצרוך תזונה מתאימה כדי למנוע חסימה של הצינור. שתייה של משקאות תוססים לאחר האכילה עוזרת לשמור על הצינור פתוח ונקי.
טיפול בלייזר
לעיתים ניתן להסיר חלק מהגידול בעזרת לייזר, וכך לאפשר מעבר קל יותר של מזון בוושט. לרוב הטיפול ניתן בהרדמה מקומית ולא דורש אשפוז בבית החולים, אך לפעמים הוא מתבצע בהרדמה כללית. לצורך הטיפול משתמשים באנדוסקופ, בדומה לאסופאגוסקופיה. הטיפול נמשך כ-15 דקות. ייתכן שיהיה צורך בשניים או שלושה טיפולים עד שהוושט יהיה נקי בצורה מספקת שתאפשר בליעה רגילה. אפשר שיידרשו טיפולים נוספים לאחר ארבעה עד שישה שבועות. כאב לאחר הטיפול אינו נפוץ, אולם תיתכן נפיחות זמנית בוושט. ייתכנו גם קשיי בליעה משמעותיים יותר לאחר הטיפול ואי-נוחות בבטן. בכל מקרה, אם יש כאב חשוב לדווח על כך לצוות הרפואי או הסיעודי.
ניתוח
ישנם סוגים שונים של ניתוחים לסרטן הוושט. הצוות הרפואי יציג את סוג הניתוח המתאים ביותר כדי לקבל החלטה על ביצועו בהתאם לסוג הסרטן ולשלב המחלה, למצב בריאותך הכללי ולהעדפות שלך. אם מדובר בגידול בשלב מוקדם, ייתכן שיוצע ניתוח שמטרתו ריפוי המחלה. חשוב לדון על כל פרטי הניתוח עם הצוות הרפואי בטרם הוא מבוצע, ולכן מומלץ להכין רשימת שאלות מראש. לא יבוצע כל ניתוח או טיפול אחר ללא הסכמת החולה. חלק מסוגי הניתוחים מצריכים שהות למשך כמה שבועות בבית החולים.
ניתן להפנות שאלות למומחים בכל הנושאים הקשורים לניתוחים של סרטן הוושט ב'פורום כירורגיה של סרטן ושט, קיבה ומערכת העיכול'
לפני הניתוח
הצוות הרפואי יוודא לפני הניתוח כי מצבך הפיזי מאפשר ביצוע ניתוח. לרוב תתקיים פגישה גם עם הרופא המרדים לפני הניתוח, וייערכו בדיקות כדי לבדוק את מצב בריאות הכללית ואת תפקודי הלב והריאות. בדרך כלל מגיעים לבית החולים בבוקר היום שבו יתבצע הניתוח. אם קיים קושי באכילה וירידה במשקל, יינתן לך הסבר בנוגע לתזונה כהכנה לקראת הניתוח.
ברוב המקרים לא יתאפשר לשתות ולאכול שש שעות לפני הניתוח.
למעשנים מומלץ לנסות להיגמל או לפחות להפחית את כמות העישון לפני הניתוח, כדי לצמצם את הסיכון לדלקת ריאות, ולסייע לריפוי מהיר יותר של חתך הניתוח.
סוגי הניתוחים
ישנם שני סוגי ניתוחים עיקריים:
כריתה תת-שלמה של הוושט (Sub-total Esophagectomy) - הסרת החלק העליון של הקיבה וכשני שלישים מהוושט, והעלאת הקיבה לחזה העליון או לצוואר לשימור המשכיות מערכת העיכול.
כריתה חלקית של הוושט והקיבה (Distal Esophagectomy-proximal Gastrectomy) - אם הגידול נמצא בחלק התחתון של הוושט, או אם הוא התפשט לקיבה, הניתוח יכלול הסרה של החלק העליון של הקיבה יחד עם החלק הנגוע בוושט. הוושט יחובר לחלק הנותר מהקיבה. במהלך הניתוח יבדוק המנתח את האזור סביב הוושט, ויסיר חלק מבלוטות הלימפה. הליך זה נקרא "הסרת בלוטות לימפה" (Lymphadenectomy), והוא נעשה משום שייתכן שהבלוטות נגועות בסרטן. הבלוטות שהוסרו ייבחנו תחת מיקרוסקופ. הסרתן מסייעת בהפחתת הסיכון לחזרתה של המחלה, וכן מסייעת לרופאים לדעת מהי דרגת המחלה.
הגישה למקום המדויק בניתוח ושט היא קשה מבחינה טכנית, מאחר שהוושט עובר בשלושה אזורים אנטומיים נפרדים: צוואר, חזה ובטן, ולעיתים יש לפתוח כל אחד מהחללים האלה כדי להגיע לוושט. בהתאם למיקום הגידול בוושט, יבחר המנתח לבצע את הניתוח באחת מהשיטות הבאות:
- כריתת ושט דרך בית החזה (Trans-thoracic Esophagectomy) - בהליך זה נעשים חתכים בבטן ובבית החזה, כך שניתן להסיר את החלק הסרטני בוושט. לעתים ייעשה גם חתך שלישי בצוואר.
- כריתת ושט בגישה בטנית-צווארית (Trans-hiatal Esophagectomy) - בהליך זה נעשים חתכים בבטן ובצוואר כדי להסיר את החלק הנגוע בוושט.
- כריתת ושט בשיטה זעיר פולשנית (Minimal-invasive Esophagectomy) - בהליך זה הכניסה לבטן ולחזה נעשית דרך מספר חתכים קטנים, דרכם מכניסים מצלמה ומכשירי עבודה ומבצעים את רוב הניתוח בלי פתיחה מלאה של החזה או הבטן. בסוף הניתוח מגדילים את אחד החתכים בחזה או בבטן כדי להוציא את החלק שהוסר בניתוח.
לאחר ניתוחים אלו מיקומה של הקיבה יהיה גבוה יותר (מעל לשריר הסרעפת המפריד בין החזה לבטן, במקום מתחתיו). כמו כן, מכיוון שבניתוחים אלו מושכים את הקיבה מעלה כדי למלא את המקום של הוושט המוסר, הקיבה תהיה קטנה יותר, ולכן יש לאכול ארוחות קטנות ותכופות, ותיתכן תחושת בחילה במקרה של אכילה מהירה מדי.
אם לא ניתן לחבר את הקיבה עם יתר הוושט, ייתכן שיהיה ניתן להסיר חלק מהמעי הגס שיחליף את החלק של הוושט שהוסר בניתוח. הצוות יספק הסבר מפורט על הניתוח.
במקרים מסוימים, לאחר שהחל הניתוח, מתברר כי לא ניתן להסיר את הגידול מכיוון שהוא התפשט ועבר את דופן הוושט, או בשל הימצאות בלוטות לימפה נגועות. במקרה כזה המנתח עשוי להחדיר צינורית או לבצע מעקף כדי להקל את הבליעה והאכילה.
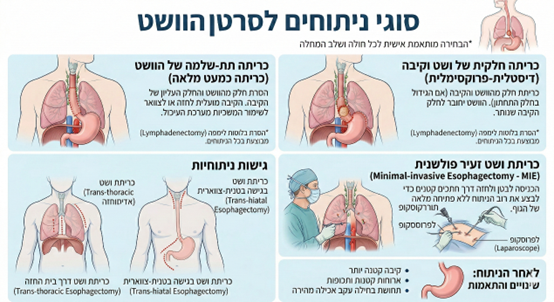
האיור נעשה באמצעות בינה מלאכותית ע"י ד"ר איהאב סמארה
לאחר הניתוח
לאחר הניתוח מרבית האנשים מטופלים ביחידה לטיפול נמרץ במשך יום-יומיים. זהו הליך שגרתי והוא אינו מעיד על מידת ההצלחה של הניתוח או על חשש מסיבוכים. בחלק מהמקרים ייתכן חיבור למכשיר הנשמה, שיסייע לנשום עד שתפוג השפעת ההרדמה. גם זה הליך שגרתי בחלק מבתי החולים.
כאב
כאב ואי-נוחות יכולים להופיע לאחר הניתוח. הצוות המטפל ייתן לך משככי כאבים וחשוב מאוד לדווח על השפעת הטיפול על הכאב כדי שהצוות יוכל להתאים את המינון ולהקל את התחושה. קיימות שיטות מגוונות מאוד לטיפול בכאב, כולל חיבור למשאבת PCA (Patient Control Analgesia) - מכשיר המאפשר מתן משככי כאבים באמצעות לחיצה על המשאבה. בכל לחיצה משתחררת מנת תרופה מתוכנתת מראש. בצורה כזאת אפשר ללחוץ על המשאבה באופן עצמאי ולשחרר כמות נוספת של משכך כאבים במידת הצורך.
למידע מפורט: כאב והטיפול בו.
עירויים וצינוריות
- עירוי: לאחר הניתוח יינתנו נוזלים דרך עירוי במשך כמה ימים עד שאפשר יהיה שוב לאכול ולשתות.
- זונדה: צינורית עדינה מאוד, העוברת דרך האף אל הקיבה או אל המעי הדק, מנקזת נוזלים ומאפשרת לאזור להחלים.
- צינוריות ניקוז לחזה ולבטן: מטרתן לנקז הצטברות אפשרית של נוזלים.
- צנתר (קתטר) לניקוז השתן: לעיתים חומרי הרדמה עלולים להשפיע על השליטה בסוגרים ועל היכולת להטיל שתן באופן ספונטני. לכן, עד אשר השפעת חומרי הרדמה תפוג, יחובר קתטר לניקוז השתן והוא יוסר כעבור כמה ימים בהתאם למצב הרפואי וכאשר יהיה ניתן להטיל שתן באופן עצמאי.
- צינורית הזנה: חלק מהמנתחים נוהגים לחבר צינורית קטנה ישירות למעי הדק, המאפשרת הזנה בזמן ההחלמה. הצינורית מוכנסת בחלקו האמצעי של המעי הדק (ג'ג'ונום) דרך חתך קטן הנעשה בדופן הבטן. הצינורית תוסר בדרך כלל לאחר 6-4 שבועות.
צינוריות אלו עלולות לגרום לתחושת אי-נוחות. במקרה זה חשוב לדווח לצוות המטפל.
פיזיותרפיה וחזרה לפעילות
הצוות הרפואי יעודד חזרה לפעילות ואף לפיזיותרפיה מוקדם ככל האפשר, שכן התנועה מהווה חלק חיוני בתהליך ההחלמה. גם בזמן שכיבה במיטה ניתן להניע את הרגליים ולתרגל נשימות עמוקות. למטופל/ת תוצע הדרכה על טיפול פיזיותרפיה שיסייע בביצוע התרגילים.
אכילה ושתייה
החזרה לאכילה ולשתייה תתבצע בהדרגה. עם זאת, תיתכן ירידה במשקל בשבועות הראשונים שלאחר הניתוח. הירידה היא נורמלית, ואמורה להיפסק בהדרגה עם החזרה לאכילה רגילה (פירוט בסעיף "תזונה" בהמשך). הירידה במשקל אינה מעידה על חזרתה של המחלה. חשוב לקבל הדרכה בנושא תזונה מתזונאי/ת בצוות. בזמן ההחלמה ייתכן גם שלשול. אם הוא מתמשך יש לפנות לצוות כדי לקבל טיפול תרופתי. לאחר הניתוח ייתכן טעם רע בפה. במקרה זה שטיפות פה עשויות לסייע.
למידע מפורט: המלצות תזונה למתמודדים עם מחלת הסרטן
תסמונת הצפה (Dumping Syndrome)
במצב רגיל, מזון מגיע מהוושט לקיבה ועובר ממנה למעי הגס באופן מבוקר. לאחר ניתוח להסרה חלקית של הוושט, ייתכן שהמזון יעבור למערכת העיכול בקצב מהיר יותר. מצב זה יכול לגרום לתסמינים הידועים בשם "תסמונת הצפה". ישנם שני סוגים של תסמונת זו: "תסמונת הצפה מוקדמת" ו"תסמונת הצפה מאוחרת".
תסמונת הצפה מוקדמת – מצב זה יכול להתרחש כ-30 דקות לאחר ארוחה. ייתכן שהוא יהיה מלווה בסחרחורת ודפיקות לב מהירות ו/או התעלפות. תסמינים אלו עלולים להימשך 15-10 דקות. לעיתים מופיעות גם התכווצויות בקיבה ושלשולים כאשר המזון עובר לקיבה בקצב מהיר. במצב זה מתרחשת ירידת לחץ דם עקב מעבר נוזלים אל המעי מהרקמות הסמוכות. ניתן להקל את התופעה בדרכים הבאות:
- אכילה איטית.
- הקפדה על אכילה של מזון יבש במנות קטנות, לעיתים קרובות.
- שתיית 8-6 כוסות משקה ביום, עדיף לא ממותק ולא מוגז וללא קפאין.
- הפרדת שתייה מאכילה – יש לשתות כחצי שעה עד שעה לפני או אחרי הארוחה ולא בזמן האכילה.
- הימנעות ממזון עתיר סוכר.
- אכילת מזונות עשירים בחלבונים (דגים, בשר וביצים) ובפחמימות עמילניות (פסטה, אורז, לחם, תפוחי אדמה).
- הקפדה על מנוחה של 30-15 דקות מיד לאחר הארוחה.
- הימנעות ממזונות או ממשקאות חמים מדי או קרים מדי.
במקרים רבים תסמונת הצפה מוקדמת משתפרת מעצמה עם הזמן.
תסמונת הצפה מאוחרת – מצב זה נפוץ יותר לאחר כריתה של הוושט, והוא מתרחש לרוב כמה שעות לאחר הארוחה, או במקרה של דילוג על ארוחה. תיתכן תחושת חולשה, התעלפות פתאומית, בחילה ורעד בשל ירידת הסוכר בדם. אפשר למנוע או להפחית את התסמינים באותן הדרכים המצוינות למעלה לגבי תסמונת הצפה מוקדמת.
ברוב המקרים חל שיפור עם הזמן בתדירות ההופעה של התסמונת והתסמינים הנלווים לה. אם התסמינים נמשכים או מחמירים חשוב לפנות לצוות הרפואי. קיימות תרופות שיכולות להקל.
השחרור מבית החולים
לפני השחרור מבית החולים תיקבע פגישת מעקב לביקורת לאחר הניתוח. בפגישה זו רצוי להעלות כל בעיה שבה נתקלת בתקופה שלאחר הניתוח.
טיפול בקרינה (רדיותרפיה)
בטיפול זה נעשה שימוש בקרינה מייננת בעוצמה גבוהה להשמדת תאים סרטניים, תוך גרימת נזק מועט ככל האפשר לתאים בריאים. טיפול בקרינה מכוון לאזורים מדויקים בגוף וניתן כטיפול חיצוני או פנימי. הטיפול בקרינה מתבצע ביחידת הקרינה (מכון קרינה) של בית החולים, בכל יום מימי השבוע, וסוף השבוע מוקדש בדרך כלל למנוחה.
תוכנית הטיפול נקבעת בהתאמה אישית לכל מטופל, והטיפול אינו גורם כואב ונמשך בין 10 ל-15 דקות.
קרינה יכולה להינתן יחד עם טיפול כימי (כימו-קרינה), בדרך כלל במטופלים אשר אינם מתאימים לניתוח או בשלב הכנה לפני ניתוח. שילוב כימותרפיה בזמן קרינה גורם לגידול להיות רגיש יותר לקרינה ובכך להגיב טוב יותר.
קרינה יכולה להינתן לפני ניתוח (נאו-אדג'ובנטי) כדי לכווץ ולהקטין את הגידול או אחרי ניתוח (אדג'ובנטי) במטרה להשמיד תאים סרטניים שלא נראו בניתוח ואולי נשארו. קרינה יכולה להינתן כטיפול תומך (פליאטיבי) כדי להקטין את הגידול ולשלוט בתסמינים. לפני תחילת הטיפול ישוחח צוות מכון הקרינה איתך על אודות הטיפול, משך הזמן שלו ותופעות הלוואי.
תכנון הטיפול בקרינה
כדי להפחית ככל האפשר את הנזק לתאים הבריאים בסמוך לגידול, יש לתכנן את הטיפול בקרינה בקפידה. הביקורים הראשונים במכון הקרינה יוקדשו למטרה זו. תהליך התכנון נקרא "סימולציה", שפירושה: הדמיה. הסימולציה נעשית באמצעות מכשיר מיוחד הנקרא "סימולטור או "CT סימולטור", אשר מבצע צילום CT ומאפשר תכנון ודיוק בכיוון ומינון הקרינה. בתום עריכת המדידות הנחוצות, האזור המדויק שאליו תכוון הקרינה יסומן באמצעות עט מיוחד או דיו. סימונים אלה יסייעו לטכנאי הטיפול למקם את גופך במדויק ולכוון את הקרניים למקום הנכון. לעיתים ייעשו הסימונים באמצעות קעקוע - מדובר בסימונים זעירים ביותר שלא יהיה ניתן להסיר בתום הטיפול. הם ייעשו אך ורק לאחר מתן אישור מפורש של המטופל/ת.
אם הגידול נמצא בחלקו העליון של הוושט, תיבנה לך מסכה מיוחדת עשויה מפרספקס (סוג של פלסטיק) או רשת פלסטיק גמישה, המותאמת אישית. מטרתה של המסכה לקבע את הראש ללא תזוזה בזמן הטיפול, כדי שהקרינה תכוון במדויק לאזור המטופל. רוב המטופלים מתרגלים למסכה במהירות, ללא בעיות מיוחדות. בכל מקרה, השימוש במסכה הוא לזמן קצר, בתחילת הטיפול בקרינה. הצוות הרפואי ינחה אותך כיצד לטפל בעור באזור המיועד לטיפול. על העור להישאר יבש ככל האפשר כדי למנוע רגישות ואדמומיות. רצוי לא למרוח את האזור בתכשיר לחות לפני טיפול, כדי לא להגביר את רגישות העור.
סוגי קרינה לוושט
טיפול בקרינה יכול להינתן בשתי דרכים:
קרינה חיצונית: שיטת קרינה זו היא הנפוצה ביותר, ונעשית במכונה הנמצאת מחוץ לגוף ושולחת קרניים לעבר נקודה מסוימת בגוף.
קרינה פנימית: שימוש בחומר רדיואקטיבי הנמצא התוך מחטים/גרגירים/חוטים או צנתרים הממוקמים ישירות בתוך הגידול או בסמוך לו. השיטה נדירה מאוד בארץ ונמצאת בשימוש במרכזים בודדים.
אופן הטיפול תלוי בסוג הגידול ובשלב הטיפול. לעיתים לפני הקרינה יוחדר צינור פלסטיק לוושט כדי לשמור אותו פתוח במהלך הטיפול. הליך זה נקרא "אינטובציה והתרחבות תוך-לומינלית".
למידע מפורט: טיפול בקרינה לאזור הבטן העליונה, הוושט והקיבה.
טיפול כימי (כימותרפיה)
טיפול זה מבוסס על שימוש בתרופות אנטי-סרטניות (ציטוטוקסיות), שמטרתן להרוס את התאים הסרטניים. התרופות פועלות באמצעות הפרעה לתהליך החלוקה וההתרבות של תאים סרטניים.
כימותרפיה יכולה להינתן לפני ניתוח להסרת גידול סרטני בוושט (טיפול נאו-אדג'ובנטי), במטרה לצמצם את הגידול ולשפר את תוצאות הניתוח ולהפחית את הסיכון לחזרתה של המחלה לאחר הניתוח. כמו כן, אם קיים סיכון שהסרטן התפשט לאיברים אחרים בגוף, קבלת כימותרפיה בשלב מוקדם יכולה להעלות את הסיכוי לשליטה טובה במחלה.
כימותרפיה יכולה להינתן גם לאחר הניתוח (טיפול אדג'ובנטי), במקרה שלא ניתן להסיר את כל הגידול בניתוח, או אם קיים סיכון גבוה לחזרתה של המחלה.
כימותרפיה עשויה לשמש טיפול עיקרי במקרים שבהם הסרטן התקדם והתפשט לאזורים אחרים בגוף. במקרה זה מטרת הטיפול הקטנת היקף הגידול, הקלת התסמינים ושיפור איכות החיים. טיפול זה נקרא "כימותרפיה פליאטיבית", והוא עשוי לסייע בהקלת התסמינים ובשיפור ההישרדות ואיכות החיים. קיימות מספר תרופות כימותרפיה יעילות לטיפול בגידול בוושט, והן ניתנות במשלבים (שילובים) שונים.
כימותרפיה יכולה להינתן כטיפול בפני עצמו, או בשילוב עם קרינה או תרופות אימונותרפיות או תרופות ביולוגיות (מכוונות מטרה). שילוב של כימותרפיה עם קרינה או תרופות אחרות יכול להגביר את תופעות הלוואי. חשוב ביותר לדווח לצוות המטפל על הופעת תופעות לוואי כדי שיהיה ניתן לטפל בהן ביעילות.
למידע מפורט: 'הטיפול הכימי'.
אלה הן התרופות הכימיות הנפוצות ביותר לטיפול בסרטן ושט:
פלואורואורציל - (Fluorouracil (5FU (פלואורואורציל® - ®Fluorouracil)*
ציספלטין - Cisplatin (ציספלטין אבווה® - ®Cisplatin Ebewe)*,
קרבופלטין - Carboplatin (קרבופלטין® - ®Carboplatin)*
קפציטאבין - Capecitabine (קסלודה® - ®Xeloda)*
פקליטקסל - Paclitaxel (טקסול® - ®Taxol)*
אוקסליפלאטין - Oxaliplatin (אלוקסטין® - ®Eloxatin)*
*או תרופות המכילות חומר פעיל זהה, בעלות שמות מסחריים אחרים.
אימונותרפיה
אימונותרפיה היא שיטת טיפול מתקדמת המגייסת את מערכת החיסון של הגוף לזהות ולתקוף תאים סרטניים באופן ממוקד. בשונה מכימותרפיה מסורתית, הפוגעת בכל תא המתחלק במהירות, תרופות אימונותרפיות פועלות על מולקולות ספציפיות המעורבות בבקרה החיסונית, כגון /PD-11-PDL או CTLA-4 ובכך מאפשרות למערכת החיסון "לפרוץ את המחסומים" שהגידול מציב בפניה.
במסגרת הטיפול במחלה גרורתית, תפסו התרופות האימונותרפיות מקום מרכזי כסטנדרט טיפולי, הן כטיפול בודד (מונותרפיה) והן בשילוב עם כימותרפיה:
- פמברוליזומאב - Pembrolizumab (קיטרודה® - ®Keytruda)*: תרופה מרכזית המשמשת למגוון רחב של התוויות גרורתיות, במיוחד כאשר קיים ביטוי גבוה של החלבון PD-L1.
- ניבולומאב - Nivolumab (אופדיבו® - ®Opdivo)*: מאושרת לשימוש במחלה גרורתית, וכן כטיפול משלים. במקרים של מחלה עם מאפייני MSI-H/dMMR ניתן לשקול את השילוב של ניבולומאב יחד עם איפילימומאב (Ipilimumab) להגברת התגובה החיסונית נגד הגידול.
- טיסלליזומאב - Tislelizumab (טבימברה®- ®Tevimbra)*: אימונותרפיה חדישה המצטרפת לארסנל הטיפולים למחלה מתקדמת וגרורתית, המציגה יעילות בחסימת ציר PD-1.
- דוסטרלימאב - Dostarlimab (ג'מפרלי® - ®Jemperli)*: תרופה שהראתה תוצאות בגידולים גרורתיים וגם כטיפול טרום ניתוחי עם מאפיינים גנטיים של חוסר יציבות גנומית (dMMR/MSI-H).
טיפולים אלה מהווים כיום את עיקר הטיפול האימוני בממאירויות הוושט, הן בסרטן תאי קשקש (ESCC) והן באדנוקרצינומה של הוושט או המפגש הוושטי-קיבתי. יעילות התכשירים האלו גבוה יותר בעת תוצאות צביעה PD1 \PDL1 גבוהה, ממצא MSI-high and\or MMR-D בתאי הגידול או TMB (tumor mutational burden) גבוה. לבירור נושא ביצוע הבדיקות להתאמה יש לפנות לרופא מטפל באונקולוגיה.
טיפול ביולוגי
טיפול זה נקרא גם "טיפול מכוונן" או "טיפול ממוקד מטרה". בטיפול זה נעשה שימוש בתרופות אשר נקשרות לקולטנים או לחלבונים הנמצאים בגידול או בתאי הגוף, כדי להביא להרס תאי הסרטן. הטיפול ממוקד נגד מטרות מולקולריות הייחודיות לתאים הסרטניים.
באופן כללי, הטיפול הביולוגי משמש לעיכוב או לחסימת הצמיחה וההתפשטות של תאי הסרטן בדומה לטיפול כימי (כימותרפיה), אך לרוב יש לו פחות תופעות לוואי לעומת כימותרפיה.
קיימים מספר סוגים של טיפול מכוונן. חלק מהתרופות פועלות במספר מנגנונים, ולכן עשויות להשתייך במקביל לסוגים שונים.
טיפולים מכוונים 2 HER
טרסטוזומאב - Trastuzumab (הרצפטין® - ®Herceptin)* - תרופה מסוג "נוגדן חד-שבטי", הפועלת על ידי היצמדות לקולטן HER2 על פני השטח של תאי סרטן מסוימים. כך התרופה עוצרת את החלוקה והגדילה של התאים הסרטניים. התרופה ניתנת במקרים של סרטן ושט מתקדם באזור החיבור של ושט-קיבה מסוג אדנוקרצינומה וכאשר בבדיקת התאים נמצא ביטוי יתר של קולטן HER-2. תרופה זו ניתנת בשילוב עם כימותרפיה.
*או תרופות המכילות חומר פעיל דומה, בעלות שמות מסחריים אחרים.
טרסטוזומאב דרוקסטקאן - Trastuzumab deruxtecan (אנהרטו® - ®Enhertu)* - תרופה השייכת לדור חדש של טיפולים ביולוגיים הנקראים נוגדן מצומד לתרופה (ADC - Antibody-Drug Conjugate). הטכנולוגיה פועלת כ"סוס טרויאני": הנוגדן נצמד לקולטןHER2 על פני התא הסרטני כאשר הוא נושא איתו חומר כימותרפי חזק במיוחד. לאחר ההיצמדות, התרופה חודרת לתוך התא ומשחררת את הכימותרפיה ישירות בתוכו, מה שמגביר את יעילות הטיפול ומפחית חלק מתופעות הלוואי המאפיינות כימותרפיה רגילה. אנהרטו ניתנת לרוב כקו שני או שלישי לאחר התקדמות המחלה תחת טיפול ב-Trastuzumab . נכון לתאריך עדכון המידע אנהרטו אינה רשומה בסל הבריאות לסרטן ושט.
טיפול מכוון Claudin 18.2
זולבטוקסימאב – Zolbetuximab (וילוי® - ®(Vyloy* - תרופה ביולוגית חדשנית המיועדת לטיפול באדנוקרצינומה מתקדמת של הוושט ומעבר הוושט-קיבה. התרופה היא נוגדן חד-שבטי המכוון נגד החלבון Claudin 18.2 (CLDN18.2) המהווה מרכיב במבנה התא ומבוטא בשיעור גבוה על פני תאי הגידול. עם היצמדות הנוגדן לחלבון המטרה, הוא מפעיל את מערכת החיסון להשמדת התא הסרטני באמצעות מנגנונים של רעילות תאית תלוית נוגדנים (ADCC) ורעילות תלוית משלים (CDC). הטיפול ניתן לרוב בשילוב עם כימותרפיה בקו ראשון עבור חולים שאצלם הגידול הוא HER2 שלילי ומציג ביטוי חיובי של הסמן Claudin 18.2 בבדיקה הפתולוגית. נכון לתאריך עדכון מידע זה וילוי אינה רשומה בסל הבריאות לסרטן ושט.
טיפול מכוונן VEGF
רמוסירומאב – Ramucirumab (סירמזה® - Cyramza®)* - תרופה ביולוגית הפועלת לעיכוב צמיחת הגידול דרך פגיעה באספקת הדם שלו. מנגנון הפעולה של התרופה כולל היצמדות סלקטיבית לקולטן VEGFR2 המצוי על פני תאי האנדותל המצפים את כלי הדם. על ידי חסימת קולטן זה, התרופה מונעת מהחלבון VEGF (גורם גדילה של אנדותל כלי דם) להיקשר אליו, ובכך בולמת את תהליך האנגיוגנזה – יצירת כלי דם חדשים הדרושים לגידול לצורך הזנה, חמצון והתפשטות. בסרטן הוושט והקיבה, רמוסירומאב משמשת לרוב כטיפול בקו שני, בדרך כלל בשילוב עם הכימותרפיה פקליטקסל. נכון לתאריך עדכון מידע זה סירמזה אינה רשומה בסל הבריאות לסרטן ושט.
שינויים גנטיים נדירים
איחוי גנטי של NTRK 1/2/3: עבור מטופלים שאצלם מזוהה איחוי (Fusion) בגנים אלו, קיימות תרופות המסוגלות לעצור את צמיחת הגידול באופן ממוקד, כגון אנטרקטיניב Entrectinib – (רוזליטרק® - ®Rozlytrek)* לרוטרקטיניב – Larotrectinib (ויטראקבי®- ®Vitrakvi)*) או רפוטרקטיניב Repotrectinib ( אוגטירו – Augtyro).
נכון לתאריך עדכון מידע זה התרופה רפוטרקטיניב אינה רשומה בארץ וממילא אינה נמצאת בסל בריאות.
מוטציית BRAF V600: אם מזוהה מוטציה ספציפית זו, ניתן להשתמש בשילוב של התרופה דבראפניב - Dabrafenib (טפינלר® - ®Tafinlar)* יחד עם התרופה טרמטיניב - Trametinib (מקיניסט® - Mekinist®)*.
נכון לתאריך עדכון מידע זה שתי התרופות לא נמצאות בסל הבריאות לסרטן הוושט.
איחוי גנטי של RET: עבור גידולים המציגים איחוי בגן RET ניתן לטפל בתרופה סלפרקטיניב (Retevmo®). נכון לתאריך עדכון מידע זה התרופה לא נמצאת בסל הבריאות לסרטן הוושט.
רפואה משלימה ומשולבת
המונח רפואה משלימה (משולבת, אינטגרטיבית) מתייחס למגוון טיפולים, כגון דיקור סיני (אקופונקטורה), נטורופתיה, דמיון מודרך ועוד, הניתנים בנוסף על הטיפולים הרפואיים המקובלים נגד מחלת הסרטן. מחקרים מראים שגישת הטיפול האינטגרטיבית עשויה לתרום לשיפור איכות החיים של מטופלים בתקופת ההתמודדות עם המחלה והטיפולים.
אם ברצונך להיעזר בטיפולי רפואה משלימה, חשוב להתייעץ עם האונקולוג/ית ועם רופא מומחה ברפואה משלימה כדי לבחון מהי דרך הטיפול הטובה ביותר עבורך, ואם שיטות רפואה משלימה עשויות לסייע בהשגת יעדי הטיפול.
מעקב
לאחר השלמת הטיפול מתחילה תקופת החלמה. בתקופה זאת יתבצעו בדיקות מעקב שגרתיות, הכוללות בדיקות דם וצילומי רנטגן. פגישות המעקב הן הזדמנות טובה לשוחח עם הרופא על חששות ולקבל תשובות על שאלות שונות. אם בין פגישות המעקב מבחינים בתסמינים חדשים או בבעיות אחרות, יש לדווח לרופא או לפנות אל בית החולים בהקדם האפשרי.
ביקורי המעקב צריכים להתרכז בתסמינים, בליווי תזונתי ובתמיכה פסיכו-סוציאלית. לעיתים קרובות נדרש צוות רב-תחומי במהלך שלב המעקב, בתיאום עם הרופא שפוגש את המטופל על בסיס קבוע. רופאים עשויים להמליץ על מעקב כל 3 עד 6 חודשים בשנתיים הראשונות לאחר הטיפול, כל 6 עד 12 חודשים במשך 3 השנים הבאות, ולאחר מכן פעם בשנה לאחר מכן. רופאים מסוימים עשויים לייעץ על לוחות זמנים שונים למעקב.
הישנות הגידול
אם הגידול חוזר, אופן הטיפול בו יהיה תלוי בשלב הגידול ובמצב הבריאותי הכללי.
גידולים משניים
קרינה באזור בית החזה עשויה לעלות את הסיכון לגידולים סרטניים משניים, כגון סרטן חלל הפה, סרטן תיבת הקול, סרטן ריאות, סרטן בלוטת התריס וסרטן המעי הדק (עקב המיקום האנטומי של המעי הדק בבטן העליונה).
רוב המומחים אינם ממליצים על בדיקות לאיתור סרטן משני אלא אם כן קיימים תסמינים. אנשים שטופלו בסרטן הוושט ואין להם סימני הישנות מחלה, אך הם מעשנים, יכולים להתייעץ עם הרופא/ה על בדיקה לאיתור סרטן הריאה.
לפורומים של האגודה בנושאים שונים, בהם ניתן להפנות שאלות למומחים.
לדף המידע: "מדריך למחלימי סרטן - עם הפנים לעתיד".
מחקרים קליניים
מחקרים למציאת דרכים חדשות לטיפול יעיל בסרטן נערכים כל העת.
מחקרים כאלה נקראים מחקרים קליניים (או ניסויים קליניים) והם הדרך האמינה היחידה לבחינת טיפול חדש. לעיתים קרובות משתתפים במחקרים האלה כמה מרכזים רפואיים בארץ, ובדרך כלל גם מרכזים רפואיים במדינות אחרות.
מחקרים קליניים חשובים לא רק לשיפור הטיפול לטובת כל המטופלים בעתיד, אלא גם מעניקים סיכוי אמיתי לשיפור מצב המשתתף או המשתתפת במחקר. כמו כן, הם תורמים לקידום המאבק במחלת הסרטן ולהעמקת הידע הקשור למחלה. אם שיטת הטיפול הנבדקת במחקר מסוים תוכח כיעילה, היא עשויה להיות שיטת הטיפול המקובלת ולעזור לחולים רבים נוספים. יעילותם של רוב הטיפולים הנמצאים כיום בשימוש הוכחה בעבר במסגרת ניסויים קליניים.
אין מידע מוכח שהטיפול החדש הנבדק במחקר יביא לידי תוצאות טובות יותר, אך מקובל להציע טיפול חדש רק אם יש סיכוי סביר שתוצאותיו יהיו טובות יותר מהטיפול המקובל.
למידע נוסף על שלבי המחקר הקליני ועל השתתפות במחקר קליני, ראו כאן
לאגודה למלחמה בסרטן מאגר של מחקרים קליניים, המתעדכן באופן קבוע.
במאגר מרוכזים מגוון המחקרים הקליניים המתבצעים במרכזים הרפואיים בישראל. המחקרים פתוחים לציבור המטופלים על פי תנאי הקבלה המפורטים בכל מחקר. ניתן לקבל פרטים ומידע נוסף במרכז המידע של האגודה בטל': 03-5721608 או בדוא"ל: info@cancer.org.il